
仲野 徹先生
|
▼1個の受精卵から
大阪大学の生命機能研究科長の仲野でございます。やや大層ですが、『生命をつくりかえる』というタイトルでいろいろお話をしたいと思いますが、ここに書いてありますように、副題にある「リプログラミング」とは「初期化」と呼ばれる現象で、iPs細胞を作ったりする時の現象なんですが、そのお話をした後に、ES細胞、そして─本当にあるかどうか判りませんが─今話題になっているSTAP細胞についてお話をさせていただこうと思います。
また、その話とは関係せずに、「エピジェネティクス」という現象についてもお話させていただこうと思います。生命をすり替える、─リプログラミングでいろんな細胞を初期化できる─のですが、やはりそういった現象よりは遺伝子そのもののほうが重要だと思います。ですので、現状では何が問題なのか、これからどういったことを考える必要があるのかについて、話題提供のような形でお話させていただこうと思います。
私自身は大阪大学大学院の医学系研究科(医学部)と生命機能研究科の両方に所属しています。今日は私自身の細かい実験の話をするつもりはないんですが、いろんな細胞がどうやってできてくるのかについて研究を行っております。いろいろ聞き慣れない言葉が出てくるかもしれませんが、できるだけ解りやすく話していこうと思いますので、よろしくお願い申し上げます。
まず、私自身は「細胞がどのようなプロセスを経て発生してくるかという研究をしている」と申し上げましたが、言うまでもなく、われわれの身体を構成する膨大な数の細胞は、もともとはたった1個の受精卵、すなわち精子と卵が一緒になった1個の細胞からできてくる訳です。では、いったいこれが何個の細胞にまで増えるのか? 実際に数えた人はいないと思いますが、少なくとも、計算上は60兆個ぐらいの細胞で成り立っていると言われています。細胞の種類も数え方によってずいぶん違うんですが、一般的にはずいぶん前から約200種類と言われています。それ以降ずいぶん研究が進んでいますので、おそらく200と300の間ではないかと思います。ですから、われわれの身体は、たった1個の細胞からどんどんと分裂を繰り返していって、最終的には200〜300種類の60兆個の細胞からできあがっている訳です。
非常に有名な実験があります。核移植の実験の一番基になっているのがジョン・ガードン卿の実験です。2012年、彼は山中伸弥教授と一緒にノーベル賞を貰われましたが、5、60年前、まだ大学院生の時にされたのが、このカエルの核移植の実験です。最近はあまりカエルの卵を見る機会はなくなりましたが、見られた方はご存知だと思いますが、カエルの卵は結構大きく、ミリ単位の大きさがあるので、非常に実験がしやすいのです。彼がどういう実験をされたかといいますと、まず紫外線をカエルの卵に照射してやります。われわれの遺伝情報はDNAの中に含まれていますが、このDNAが、紫外線を当てることによってチョンチョンに切れてしまいます。そうすると、遺伝子として機能しなくなりますが、ジョン・ガードン卿の実験は、そうやってもともと卵の中にあった遺伝子を駄目にしておいて、そこへ別のカエルの腸の細胞の核を入れてやるというものです。そうすると、ちゃんとカエルができました。
 ジョン・ガードン卿の実験
ジョン・ガードン卿の実験これがその写真なんですが、別のカエル由来の遺伝子が発現したことがすぐに判るように、アルビノと呼ばれる色素が作れない別のカエルのオタマジャクシの腸の細胞から核を取ってきて、色素を作る普通のカエル――「カエル」と申しましても、普段われわれが見るような舌を伸ばして餌を捕食するようなカエル――ではなく、アフリカツメガエルというちょっと下等なタイプです。その茶色い体色を持っているカエルの卵の核の遺伝子を壊しておいて、白いアルビノタイプのオタマジャクシの腸の細胞の核を入れてやると、白いオタマジャクシができてきました。ということは、核の中に遺伝情報が入っているということが判ります。もうひとつは、成長して腸の細胞としてしか機能しないようにプログラムされた細胞も、卵の中に戻されると、もう一度、どんな細胞にもなることができるようになる。言ってみれば先祖返りのようなものです。そういった現象をリプログラミングと呼びます。
▼核移植クローンは異常が発生する
もうひとつ有名なのが、15年ぐらい前になりますが、世界で一番有名な羊といわれている「クローン羊のドリー」の話です。これも基本的には同じやり方です。先程のカエルの研究が50年ぐらい前ですが、哺乳類で核移植によるクローン動物を作るのは非常に難しいのではないかと言われていました。1980年代に「ネズミで核移植クローン動物ができる」という報告がされたんですが、これは完全に捏造だったんです。捏造だったからできないという訳ではないですが、そういう経緯もあって多くの人が哺乳類は非常に難しいのではないかと思っていました。しかし、ずっと続けていた方が居てできるようになりました。この場合は紫外線を当てるのではなく、細胞の核を取り除きます。
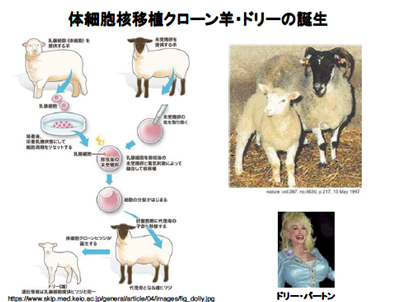 体細胞核移植クローン羊・ドリーの誕生
体細胞核移植クローン羊・ドリーの誕生クローン羊ドリーの場合は、乳腺の細胞が使われました。乳腺の細胞はミルクを作る機能しか持っていないのですが、この細胞の核を、核を取り除いた卵の中に入れてやったものを、カエルの場合と違って非常にややこしいのは、子宮の中に戻してやらなければ駄目な点でした。この作業を何度も根気よく繰り返した結果、何十頭に1頭の割合でようやく子供が産まれました。それがドリーです。余談ですが、ドリーという名前はどうして付けられたかといいますと、乳腺から取られた細胞を元に実験したので、僕もあまり知りませんが、巨乳で有名なドリー・パートンという女優さんの名前を取って「ドリー」と名付けられたそうです。
核移植クローンと言いますと、一昨日のSTAP細胞の記者会見に出てこられて大活躍された、STAP細胞論文の共同執筆者のお1人の若山照彦先生が、おそらく世界中で核移植クローン動物を作るのが一番お上手だと思います。記者会見をご覧になられたら分かりますように、非常に実直な先生で、良い意味でも悪い意味でも職人さんみたいな先生です。僕も非常に親しいですが、あの先生が悪いことをされるようなことは絶対ないと思います。この先生は、世界初のマウスの核移植クローンを成功された先生です。
 マウスの核移植クローニング
マウスの核移植クローニングこちらが核移植クローン、こちらが正常なマウスですが、見ていただくと分かりますように、核移植クローンをしたマウスは、どうも肥満のマウスが多いということが判っています。核移植をすると、いろんな異常、いろんな病気が起こりますが、ドリーも結局関節炎か何かが酷くなったため、ヒツジとしての天寿を全うすることなく安楽死で殺されました。これがDNAの異常、あるいは遺伝子の異常であれば、この太った状態が子供に遺伝するはずです。ところが、核移植クローンで作った太ったマウス同士を掛け合わせれば、また肥満のマウスができるかというと、正常なマウスが産まれます。ということは、核移植クローンをした時に遺伝子に異常が起きたのではなく、他の何かに異常が起きて肥満になったと考えられます。これが今日のお話のテーマのひとつであるエピジェネティクスであろうと考えられます。これは後ほど詳しくお話いたします。
▼初期化と全能性
これは言葉の定義ですが、リプログラミングを「初期化」といいますが、これは先ほどの話にも出てきたような、細胞分裂の結果、いったん乳腺に分化した細胞、あるいは腸に分化した細胞が、もう一度どんな細胞にでもなれる(非常に初期の状態に戻る)ことを日本語でこう呼びます。よくコンピュータが駄目になった時に、いったんすべてのプログラムを消去して、再度インストールし直すことを「初期化する」と言いますが、「初期化」とは生物学的にはプログラムをもう一度書き換えるという意味になります。
次に「全能性」という言葉がありますが、全能性とは何かと申しますと、これからいくつか出てきますが、「すべての細胞へと分化できる能力」です。最初に申し上げましたが、精子と卵が一緒になった細胞である受精卵は、その後、200ないし300種類あると言われる全部の種類の細胞になれるので「全能性」という言い方をします。
もうひとつ似た言葉で「多能性」という言葉があります。これは「2つ以上、ほぼすべての細胞へと分化できる能力」ですが、言葉を変えれば全能性から1つか2つ欠けても多能性になります。これからお話するES細胞やiPS細胞は、全能ではありません。
マスコミではよく「万能性」という言い方をされますが、これはあくまでもマスコミ用語です。万能というと「万能包丁」とか「万能ネジ」といった商品として何かに便利に使われて初めて万能ですが、まだ全く臨床に応用されていないのに万能はなかろうという気がします。この「万能性」という言葉は、かれこれ20年近く前から使われていますが、「全能性」と「多能性」でいえば、多くの場合は多能性という言葉がマスコミでは万能性と言われているとお考えいただければと思います。僕はいつもマスコミの方に対して「万能性という言葉を使うな」と言うんですが、多勢に無勢で全く意見は通らず、ずっと「万能性」という言葉が使われ続けています。
そして、最初にお話した「リプログラミング」は何かと申しますと、ちょっと言葉だけ聞くと難しく感じるかもしれませんが、『ウィキペディア』を引くと「DNAメチル化などのエピジェネティックな標識の消去・再構成」と出てきます。ウィキペディアというと、大学では、講義でレポート課題を出す時に学生に対して、何か調べものをする時に(きちんと文献に当たらずに、ネット検索でサッと調べられる)「ウィキペディアなど使ったらあかんで!」と注意しますが、ほとんどの先生が専門外のことはウィキペディアで調べながら講義をしているという拙い状態にあります(会場笑い)。
「DNAのメチル化」も「エピジェネティックな標識の消去・再構成」も何のことか判らないと思いますが、これは後ほどお話させていただきますが、もう少し平たく言いますと「分化した細胞や核が、全能性あるいは多能性を再獲得する現象である」となります。ですから、先程申し上げたジョン・ガードン卿の実験であれば、オタマジャクシの腸の細胞の性質しか出されないようにプログラムされているものが、もう一度全部の細胞になれるような全能性になることであり、ドリーの例でいえば、ミルクしか作れないようになった細胞の核がもう一度どんな細胞にもなれる。これは厳密に言えば多能性なんですが、そういった細胞になれることがリプログラミングです。
余談になりますが、こういう仕事をしている関係で、STAP細胞疑惑が表沙汰になった4月頃に一杯テレビやラジオに出まして、何度も解説させていただきました。私は、STAP細胞に関しては、初めから「ないだろう」と思っているんですが、丹羽仁史先生のこともあるので「ひょっとしたら…?」という感じで望みを完全には捨てていないというのが現在の私のスタンスです。とはいえ、昨日、一昨日の報道を見ていたら「本当にあるなら嘘を付くはずないわな…」という気もしますので、やはり、「STAP細胞は存在しないのかな…」という気持ちにもなります。
▼研究成果を実際に役立てるのは…
少しだけ私の研究の話をしますと、私自身はES細胞あるいはiPS細胞から試験管の中で血液の細胞を作るという実験を長年やっております。再生医学においては「ES細胞やiPS細胞を足りない細胞に使ってやる」と言いますけれど、これらの細胞を直接移植する訳ではありません。と申しますのは、直接移植してしまうと、ある種の腫(=細胞のかたまり)を作ってしまうので、かえって病気を作ってしまう…。ですので、必ず先に試験管内で望みの細胞に作り替えてから移植するプロセスが必要となります。つまり、神経を足したい時は、まず試験管内で神経の細胞を作りますし、血液の細胞を作りたい時は試験管内で血液の細胞を作るといった試験管内の分化誘導のプロセスが非常に大事なのです。
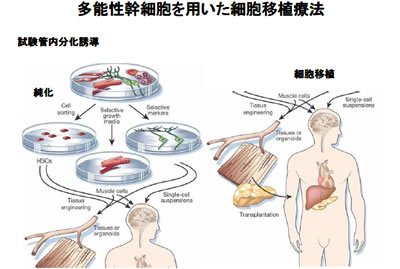 多能性幹細胞を用いた細胞移植療法
多能性幹細胞を用いた細胞移植療法私自身は20年前にOP9という細胞の上でES細胞を培養すると血液細胞ができるという方法論を確立することができましたが、もうひとつは、私がちょっと教えてあげた「違う細胞の上で培養すると神経細胞ができる」ということを見つけたのが、小保方さんと共に話題に上っている笹井芳樹先生(註:その後、8月5日に自殺)です。彼は、小保方さんの直接の上司であったため、今では凄い悪者のように言われていますが、私より5歳下の笹井先生は非常に優秀な人で、大学院生の頃から本当に優秀でした。ノーベル賞を取られた山中先生と笹井先生とどちらが優秀かというと、私は笹井先生のほうがだいぶ優秀ではないかという気がします。何をもって優秀というかにもよるかもしれませんが…。
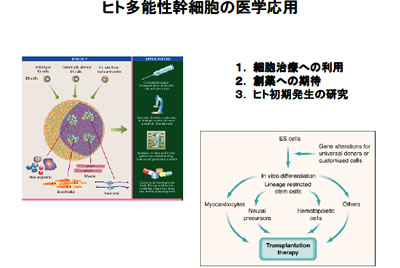 ヒト多能性幹細胞の医学応用
ヒト多能性幹細胞の医学応用現在、一番進んでいるのが神戸の理研CDB(発生・再生科学総合研究センター)で、高橋政代先生がやっておられる失明した患者さんにiPS細胞を使って網膜色素細胞を作って移植し、目が見えるようになるかどうかという研究開発プロジェクトです。ただ、あれは臨床試験というよりは、安全性の試験ですね。本当にそういうことをしても安全かどうかが確認されるのが、今年の終わりか来年の初め頃(註:実際には、本年9月12日に成功)と言われています。ES細胞技術も樹立されてから15年以上経ちますけれども、いくつか方法がありますが、それが臨床的に使われて実際に病気が完全に良くなったという報告までは一度もありませんでした。研究とはそれぐらい時間がかかるものだとお考えいただいたほうが良いと思います。
▼エピジェネティクスとは
ここで話題を変えて、次は今日のもうひとつのテーマであるエピジェネティクスについてお話ししようと思います。聞き慣れない言葉だと思いますが、この「エピジェネティクス」という言葉を理解するための用語を簡単に説明したいと思います。「DNA」という言葉はよく耳にしますでしょう? コマーシャルで「ホンダDNA」と言われると「なんのこっちゃ、車にはDNAないやろ」と思いますが(会場笑い)。DNAは物質名で、化学名はデオキシリボ核酸という高分子生体物質です。100%ではないのですが、ほぼ全ての遺伝情報が細胞核内のDNAに蓄えられています。ですから、親から子へ形質が遺伝するのですから、もし、DNAに異常がある場合には遺伝病が起きるという訳です。後ほど構造に関する話が出てきますが、一般的には、DNAという長いリボン状の物質の上に、A(アデニン)、C(シトシン)、G(グアニン)、T(チミン)という4つの塩基によって文字が書かれていると考えていただいても良いと思います。
「ゲノム」という言葉も時々聞かれると思いますが、細胞の核の中に入っている遺伝情報全部を「ゲノム」といいます。では、われわれの体の1個1個の細胞の中に、DNAはどれぐらいあるのかというと、実際に測った人はいませんが、計算上、長さにすると1.8メートルと言われています。これが46本の染色体に分かれているんですが、そこに約60億個のACGTの塩基がずらっと並んで遺伝情報を蓄えています。よく「遺伝子DNA」という言い方を耳にしますが、ゲノムとはひとつの細胞の中にある全遺伝情報(DNAのACGTの並び方)のことです。遺伝子というのはDNAと同義語で使われることもよくあるんですが、もう少し厳密な定義でいうと、タンパク質をコードする(註:塩基対が3つで一組の「文字」としての情報を記録し、20種類あるアミノ酸のどれをどのような順番に並べてタンパク質を合成するかということを決めている)核酸の単位を遺伝子と呼びます。
ヘモグロビンや色素の遺伝子など、遺伝子にもいろいろありますが、からだ中のどの細胞もすべて同じゲノムを持ってます。それは、全能性の受精卵であろうが、分化した神経の細胞であろうが、ひとつの生物個体におけるゲノムはすべて全く同じです。言い換えれば、60億個のACGTの並び方がすべて一緒だということです。
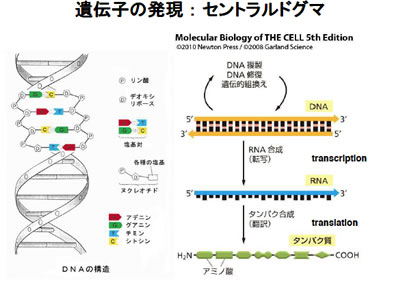 遺伝子の発現:セントラルドグマ
遺伝子の発現:セントラルドグマこの60億個が生命の設計図なんですが、その内、有効な遺伝子はその中のたかだか2万個ぐらいです。ですからタンパク質としてはだいたい2万種類ぐらいしか作られません。先程申し上げましたように、細胞には受精卵、未受精卵があり、神経の細胞、血液の細胞、筋肉の細胞といったいろいろな細胞がありますが、2万個の遺伝子によって全てが読まれている訳ではなく、対象となるのはだいたい2,000個から3,000個ぐらいだろうと言われています。ですから、どの遺伝子が読まれているかによって、血液の細胞、神経の細胞、筋肉の細胞であるかが決まっています。言い換えますと、全能性の細胞というのは将来的に何でも読めるような細胞になる訳です。けれども、実際には、どんどんと受精卵から分裂して、形ができてきて個別の機能を持つ段階で、特定の遺伝子しか発現しなくなっていきます。それが「細胞の分化」です。
次に「ヒストン」ですが、これはDNAが巻き付いているタンパクです。DNAは先程申し上げましたように、1.8メートルもあるリボンのような物質ですから、そのままポンと何ミクロンもない核の中に入ってしまうともつれてしまう可能性があるので、かつては糸巻きみたいに巻き付いてコンパクトに入っていると考えられていました。個別の機能を持った細胞に分化する際に、これを巻き戻して「どの遺伝子を読みなさい」ということを指示するのもヒストンが決めているということが、最近判ってきました。これがエピジェネティクスです。
DNAは二重螺旋構造で、Aの向かい側がT、Cの向かい側がGと決まっていますが、それが直接タンパク質を作るのではなく、いったんDNAから転写されたRNAが作られて、それをさらに写して最終的にタンパク質が作られて機能するようになります。そして、どのタンパク質が発現するかによって細胞の性質が完全に決まります。では、エピジェネティクスとは何かというと、「DNA塩基配列の変化を伴わずに、染色体における変化によって生じる、安定的に受け継がれうる表現型」と定義づけることができます。
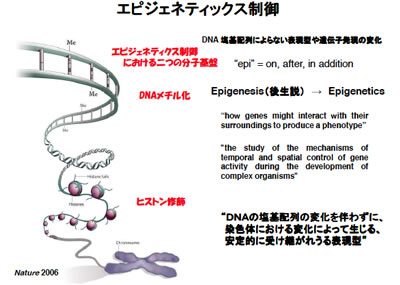 エピジェネティクス制御
エピジェネティクス制御ACGTの並びに突然変異が起きると、当然その細胞の性質は変わりますが、そうではなく、ACGTの並び方が変わらないにもかかわらず、細胞の性質が変化していく。先程申し上げましたように、われわれの体のACGTの並び方は、全能性の細胞から特殊な細胞までまったく一緒なので、実際に細胞が機能するためには、「どの遺伝子を読みなさい」、「どの遺伝子を読んではいけない」といったことが、いちいち決められている訳です。そのACGTの並び方は変わらないけれども、細胞の性質が変わったりする時、それをコントロールしているのがエピジェネティクスであり、ひとつの性質です。その科学的なものを「ヒストン修飾」と呼びます。DNAは糸巻きのようにクルクルッとだいたい2回ずつぐらい巻き付いていますが、こういう構造をとって最終的に染色体になっています。もうひとつは、DNAにメチル基(炭素に水素が3つくっついた物質。化学記号ではCH3)がくっつくことで遺伝子の読まれ方が決まっています。それが「エピジェネティクス制御」です。
▼ゲノムを上書きするもの
コンラッド・ワディントンという人がエピジェネティクスという言葉や概念を最初に作った人ですが、それを説明する時に使ったのがこの図です。このように地形をイメージして考えるんですが、スマートボールの台をイメージしていただくと判りやすいかもしれません。向こう側(全能性)が高く、手前(分化した細胞)が低くなっていて、その間にはいろんな谷があります。細胞が分化する時、全能性の細胞がこの地形の谷になった部分をコロコロと転がってきて、筋肉の細胞、血液の細胞、あるいは神経の細胞になる。これをエピジェネティックな地形と考えましょうという訳です。細胞自身は変わらないけれど、それを制御しているものを、このような地形として考えてみたのです。
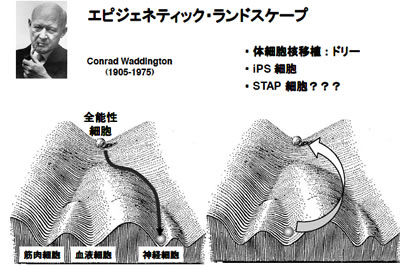 エピジェネティク・ランドスケープ
エピジェネティク・ランドスケープでは、ジョン・ガードン博士のカエル、ドリーのような体細胞核移植、山中教授のiPS細胞、そして─あるかないか判りませんが─STAP細胞をどう考えてやれば良いかというと、既に分化した細胞、あるいは分化した細胞の核が全能性(あるいは多能生)に戻るということは、本来ならば起こるはずがない訳です。というのは、地形で示されているように、向こうが高くこちらが低い訳ですから、ボールは一方向にしか転がらないのです。ところが、iPS細胞やSTAP細胞といった特殊な状況になると、手前からジャンプして再び奥へ戻るようなことが起こる。何故起こるかというと、細胞のエピジェネティックな状態が、既に分化した状態から、全能性(あるいは多能性)の状態に戻る。それを人為的にしてやるのが核移植であり、先程申し上げた山中4因子という4つの遺伝子を入れてやると、そういうことが起こるという訳です。これは細胞の分化から見たエピジェネティクスです。
このスライドは、エピジェネティクスを説明する時にいつも最初に出すものですが、タイトルの「あいのこ」という言葉はあまり良くないかもしれないので括弧を付けていますが、いわゆる動物の雑種です。雄のロバと雌のウマを掛け合わせたものは、皆様も耳にされたことがあると思いますが、ラバという名前で、粗食に耐えてよく働くので良かったんですが、逆に雄のウマと雌のロバを掛け合わせたものは、ラバがどちらかというとロバに見かけが似ているのに対して、見かけはウマに似ているものの、干し草など良いものしか食べない割に働かないので役に立ちません。そのせいか、全然作られないため、名前すら知られていませんが、ちゃんとケッテイと名前が付いています。農耕が機械で行われるようになったことで、実際にはラバも作られることはほとんどありません。雄のトラと雌のライオンを掛け合わせると必ずしもこうなるとは限りませんが、まるでCGのように頭がライオンで尾っぽがトラの模様の動物タイゴンができます。これも雄雌を逆にして雄のライオンと雌のトラを掛け合わせると、ライガーという弱っちい縞模様で、まるで阪神タイガースのようなります(会場笑い)。ただ、ライガーはトラよりもはるかに大きいので、現存するネコ科の動物では地球上最大と言われています。
 「あいのこ」の不思議:ラバとケッテイ、タイゴンとライガー
「あいのこ」の不思議:ラバとケッテイ、タイゴンとライガー何が言いたいかといいますと、先程申し上げたゲノムで言うとラバもケッテイもロバのゲノムを半分とウマのゲノムを半分持っているはずです。また、タイゴンもライガーも、トラのゲノムを半分とライオンのゲノムを半分持っています。ところが、それをお父さんからロバのゲノムを貰うか、お母さんからロバのゲノムを貰うか。あるいは、お父さんからトラのゲノムを貰うか、お母さんからトラのゲノムを貰うかで、性質が違ってくる訳です。しかし、先程申し上げたACGTの並び方というのはまったく変わらないはずです。どちらも同じゲノムを持っているのに、そのゲノムをお父さんから貰ったか、お母さんから貰ったかで性質が異なるということは、ゲノムの上にDNA以外の何らかの情報がさらに上書きされている。
先程の話ですと、ゲノムが変わっている訳ではないけれども、地形が違う(その制御が異なる)と、違う細胞になる。そういう風に考えないとおかしいですよね。それがエピジェネティクスのひとつの大きな性質です。しかし、エピジェネティクスを語る時に必ず出てくる話なのですが、完全にエピジェネティクスだということが証明されている訳ではありません。ただ、現在の生命科学の概念でいうと、エピジェネティクス以外ではちょっと説明がつかないため、エピジェネティクスという風に考えられています。
▼倹約表現型
確か昨年亡くなられたんですが、デービット・バーカーさんというイギリスの疫学者が、あることを見つけました。何を見つけたかというと、イギリスは戸籍制度が整っているため、健康情報の蓄積から非常に巧く調査できたようですが、生まれた時の体重と、5、60年経った後の冠状動脈疾患(心筋梗塞)になる率を調べてみると、何となく丸々と太った赤ちゃんのほうが、そのままずっと大人になって心筋梗塞や生活習慣病になりやすいイメージがありますが、実は生まれた時の体重が軽いほど、後年、心筋梗塞になりやすいという報告があります。
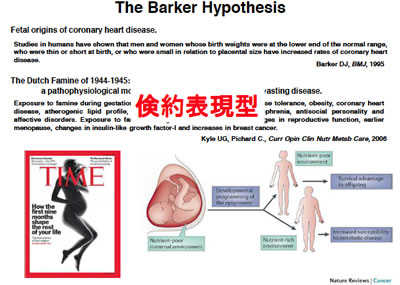 倹約表現型
倹約表現型これは常識に反するため、多くの人が「間違いではないか」と思いました。だいたい研究者というものは性格が悪くて自分の言うことは信じるけれど、他人の言うことは疑う人が多いですが、この説は世界中で追試されて調べた結果、どの国でも生まれた時の体重が軽いほど、大人になってから生活習慣病になる率が高いことが報告されています。近頃「小さく産んで大きく育てる」といってダイエットされる妊婦さんが居られますが、あれはあまり良くないと言われています。もちろん、必ずなるという訳ではなく、「生活習慣病になりやすい」という話ですが…。
この話は、もうひとつ大きなエビデンス(証拠)があります。第2次世界大戦の折、オランダも激戦地区で、亡くなった人の数は日本の亡くなられた兵隊さんの数より多いと言われていますが、1944年から1945年にかけての一番最後の冬、オランダは記録的な寒波に見舞われ、その上ナチスからも経済封鎖を受けて飢饉に陥りました。住民の摂取カロリーの平均が800キロカロリー以下となり、その結果、何万人もの人が餓死したと言われています。当時、既に妊娠しているお母さんも居られた訳ですが、お腹の中で飢饉に遭った赤ちゃんは、生まれてから50年から60年経った後調べてみると、やはり生活習慣病になりやすいということが判りました。
しかし、ゲノムは栄養状態が悪くなったからといって決して変わることはありませんから、これは決して遺伝的要因ではありません。お母さんのお腹の中で低栄養の状態に曝されると、50年間、体のどこかの細胞が覚えていて、「なんとしても栄養を取り込まなければいけない」というふうに機能するので、生活習慣病になりやすい。これは絶対エピジェネティクスだと思われます。
どの細胞がどういうエピジェネティックな状態が変化したのかは判っていませんが…。これは、「倹約表現型」と言われています。どういうことかというと、お腹の中の胎児の場合はエピジェネティックな状態が変わりやすい。妊娠初期の状態はエピジェネティックな状態がほぼ白紙の状態で、そこへ情報が書き込まれていろんな細胞になっていく訳ですが、その段階において非常に低栄養の状態に陥ると、胎児の体は「世の中は低栄養なのだな」と思ってしまい、細胞に刻まれます。これは決してDNAの塩基配列が変わる突然変異ではなく、おそらく環境要因がゲノムに上書きされることによってできたのではないかと思われます。そのままずっと死ぬまで低栄養だったら、倹約表現型が巧く機能して問題ないのですが、すぐに飢餓状況が改善されて、生まれてから普通に栄養を摂るようになると、その人は、一生涯相対的に栄養過剰になってしまうのです。というのは、「体が低栄養に適用するようにセットされてしまっている」からです。
▼ゲノムという文章のどの部分を読むのか
これはエピジェネティクスのまとめなんですが、ごく簡単に言いますと、われわれの体には、およそ2万個の遺伝子があり、そのうち200種類あまりの細胞があり、すべての細胞においてゲノムは同じだけれども、それぞれの細胞には細胞に固有の遺伝子発現パターンがあります。その遺伝子発現を制御しているのが、今申し上げたエピジェネティクスという現象です。エピジェネティクスにはヒストン修飾とDNAメチル化があり、ヒストンがアセチル化されると、遺伝子発現は活性化されます。DNAがメチル化されると、遺伝子発現が抑制されます。
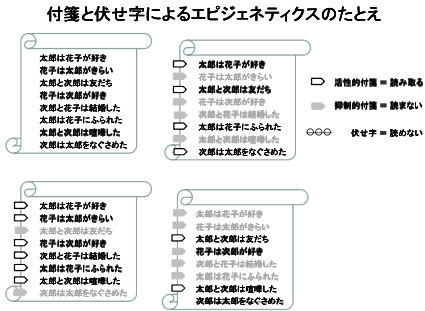 付箋と伏せ字によりエピジェネティクスのたとえ
付箋と伏せ字によりエピジェネティクスのたとえこちらの図は、今、申し上げたまとめをもう少し平たく書いたものですが、遺伝子の一本一本を文章と考えてみてください。細胞の中にゲノム(遺伝子)がダーッと並んでいる。そのどの遺伝子を読むか? 例えば、この図の左上の巻物の中のどの文章を読むかがエピジェネティクスだと考えてみてください。それぞれの文章が細胞のゲノムです。「太郎は花子が好き。花子は太郎がきらい。太郎と次郎は友だち。花子は次郎が好き。次郎と花子は結婚した。太郎は花子にふられた。太郎と次郎は喧嘩した。次郎は太郎をなぐさめた」といっぱい文章が書かれていますが、エピジェネティクスとは「ここを読んでください」あるいは「読んではいけませんよ」という付箋を付ける、もしくは伏せ字にして読めなくするようなものです。
右下の例ですと、「太郎と次郎は友だちで喧嘩した」という話になりますが、右上の「太郎は花子が好き。太郎と次郎は友だち。太郎は花子にふられた。次郎は太郎をなぐさめた」という文章だけを繋ぐと、「次郎はええ奴やったんやな」という物語ができます。けれども、左下の「太郎は花子が好き。花子は太郎がきらい。花子は次郎が好き。次郎と花子は結婚した。太郎は花子にふられた。太郎と次郎は喧嘩した」ですと、「次郎は悪い奴やったんや」という印象が残ります。元はどれも同じ文章でも、エピジェネティクスによってどの遺伝子を読み、どの遺伝子を読まないかと読み違えることによって、違う情報を読み取ることができる訳です。それが同じゲノムを持っていても、ある細胞がエピジェネティクスな状態が違うことによって、違う性質を持つということを説明するための略図なのですが、良い例えになればと思います。
DNAのメチル化についてもうひとつだけ加えますと、精子も卵子もエピジェネティックな情報がいっぱい書き込まれています。ですので、精子特有のDNAメチル化パターンと卵子特有のDNAメチル化パターンが入っています。考えてみると不思議ですよね。受精した途端に、どんな細胞にでもなれるようになる。ですから、受精した途端にDNAメチル化が、ガクンとほとんどゼロになります。全能性の細胞というのは、DNAのメチル化状態でいうと、まっさらの状態なんです。そこへ血液細胞なら血液細胞の、神経細胞なら神経細胞のメチル化パターンが書き込まれていく。これが、先程出てきた細胞がコロコロと転がっていくエピジェネティックランドスケープの図に例えられます。
次に「エピジェネティクスとは、どれぐらい大事なのか」という話に入っていきます。中には「エピジェネティクスこそが一番大事だ」と言う人も居られますが、それは微妙です。やはり、一番大事なのはゲノムです。先程申し上げたように、ゲノムがあってこそのエピジェネティクスです。先程の巻物の例えでいうと、その元となる文章がゲノムで、その文章(遺伝子)をどう読むかがエピジェネティクスです。ゲノムは普遍で、受精卵からそれぞれ個別の細胞に至るまで変わらないですし、お父さんのゲノムを半分とお母さんのゲノムの半分を受け継いで受精します。それに対して、エピジェネティクス(ゲノムをどう読むか)、あるいはエピゲノム(細胞全体のエピジェネティクスな状態をひとまとめにした言い方)は、安定しているけれども変えることが可能です。そのための薬剤は既に知られていますが、これによってエピジェネティクスな状態を変化、誘導することができます。iPS細胞は山中四因子を入れることによってエピジェネティクスな状態を初期化することができます。あるいは核移植でも、エピジェネティクス状態を初期化することができます。
「エピジェネティクスは生命観を変えるか?」というと、たいそうに言う人の中には「ゲノムだけでは判らないから、エピジェネティクスは生命観を変える」という人もいますが、そこまでは言えないのではないか…。個人的には、ゲノムのほうが圧倒的に大事だろうと考えます。ですので、どちらかといえば、エピジェネティクスはゲノム情報の読み出し機構にすぎないということです。また、先程挙げたように、薬剤で変えることができるという点も非常に大きいです。ひとつ良い例が、「骨髄異形成症候群」と呼ばれる、最近新聞の死亡記事でも時々見かけますが、高齢者によく見られる骨髄機能の異常によって起きるある種の白血病のような病気があるのですが、これに対する薬は今までなかったのですが、エピジェネティクスな状態を変えるお薬を使うと、完全には良くならないのですが、明らかに延命効果があることが判っています。
ですから、「エピジェネティックな状態を変えることによって、ある種の病気を治すことができるのではないか」という期待が寄せられています。あまり、こればかりに期待をかけるのはよくありませんが…。
▼生命科学と宗教や法律との折り合い
最後に、ゲノムについて少しお話しします。最終的にヒトゲノムの解読(全遺伝子情報の判読)がすべて判明したのは2003年のことですが、1990年に米国でヒトゲノム解読が始まった頃には、「ヒトのゲノムをすべて解読するためにかかる費用が─実際にはもっとかかったでしょうが─低めに見積もっても30億ドルと言われていました。しかし、実際には、どんどんと良い機械ができて、当初15年かかると言われた期間が13年ですべて解読されました。その後も、どんどんと新しい装置が導入されてきていることから、特定の人の全ゲノムをすべて解読するスピードも飛躍的に上がっており、おそらく10年以内には、ある人の全ゲノムは1,000ドルで読めるようになると言われています。因みに、現時点ではだいたい1万ドルから10万ドルぐらいだそうです。それでも30億ドルに比べればずいぶん安くなったと言えますが…。大枚をはたいて読んでもらった日本人はまだあまり居られませんが、アメリカでは「ベンツを買う代わりにゲノムを読んでもらおうか」という金持ちが結構いるそうです。しかし、もしヒトゲノムを読むための費用が10万円(1,000ドル)になったら、非常に多くの人が自分のゲノムを読むことを望むようになるのではないかと考えられています。
これは余談ですが、この『遺伝子医療革命』という本は非常によく書けています。著者のフランシス・コリンズという人は非常に不思議な人なんですが、この本を読むと今のゲノム医学のほとんどが判るといっていいぐらい書かれています。彼はヒトゲノム計画の責任者の1人ですが、自身はカトリックで神の存在を100パーセント信じています。どうやって折り合いを付けているのか判りませんが、宗教を信じる科学者代表で一番よく出てくるのがこの人です。この人の頭の中では、ゲノムやエピジェネティクスや発生と、神様が人間を創られたということは両立しているようです。私は、何回読んでもそれらが両立しているように思えないのですが…。それから、この『1000ドルゲノム』という本は、ちょっと内容が難しいです。割と最近出版された本なのですが…。
僕らの世代は「ゲノムのことをよく知っているか?」と尋ねられると、それほど知りませんが、おそらく今の医学生が一人前の医者になる頃には、患者さんがUSBメモリを持ってきて「先生すいません、私のゲノムはこれですねん。一番良い治療をやってもらえますか」なんていう時代が必ずやって来ると思います。しかし、そうなってくると、着床前診断の問題が出てきます。アメリカではどの宗教かは知らないのですが、ヒトのES細胞が議論される時は、5つの宗教団体から代表が出てきて議論に加わるそうです。
一方、日本では、この着床前診断に関して法整備がものすごく遅れています。日本は生命科学を法律に取り入れたのがものすごく遅かったのですが、この間、新聞で大きく取り上げられていた事件「父子の遺伝子鑑定をして一緒だったら親子と認めるのか、それとも婚姻関係があった時に生まれた子は、それを父子関係と認めるのか」というケースは、法律では定められていません。明治時代に作られた法律ですから、人工授精や不義密通をするという概念がなかった訳ですから、婚姻関係がある女性から生まれた子供は、たとえ、遺伝子上の父親が誰であれ、現在の法律では婚姻関係にある夫の子と認定されます。もっとややこしいのは、「借り腹」の場合です。現在では、別の女性から卵子を貰ってきて妊娠することも可能ですから、何を持って親子と認定するのかは、ものすごく難しい話です。
着床前診断も難しい話のひとつですが、これは8細胞期─1個の受精卵の細胞数が2個になり、2個が4個になり、4個が8個まで分裂した時期─に細胞を1個だけ取ってきて、その遺伝子を調べます。この着床前診断を使えば、男女の生み分けは確実にできます。先程の話ですと、試験管内で人工授精した卵を取ってきて、8細胞までいった時点で1個だけ細胞を取り出し、その遺伝子に異常があるかないか、あるいは男か女かを調べて、子宮に戻してやる、あるいは遺棄することは可能です。日本の産科婦人科学会が出している指針は─法律では定められていないですけれども─とても微妙な側面があります。まず男女の生み分けは認めていません。
その代わり、重症な遺伝性疾患については、着床前診断をやっても(つまり、不都合があれば遺棄しても)良いことになっていますが、これにはものすごく反対している人もいます。例えば、(3,000人に1人の割合で男児に発生すると言われている)デュシェンヌ型の筋ジストロフィーは着床前診断の対象疾患に入っているのですが、その患者団体は「それならば、われわれは生まれてくるなということか」と反対してます。これも、すでにその病気を持って生まれてきた人にしてみれば、当然の反応です。いつも医学部の学生に話すのですが、何が正解かは判りません。
しかし、医者になるからには、患者さんの言うことを聞くかどうかは別として、自分自身はどういう考えで着床前診断に賛成、あるいは反対なのかは考える必要があると思います。ただ、自分自身が反対だからといって患者さんに対して着床前診断は絶対行わないというのもおかしいと思います。ここは医師に身に付けてほしいと思う点です。こういった例は、ダウン症の場合も同じで、DNA検査などでゲノムが読まれるようになると、かなり簡単にダウン症かどうか判断できるようになりますが、技術的にできるということと、それをするということは別の問題です。
▼社会全体で考えなければならない問題
エピジェネティクスの研究は、まだそこまで進んでいませんが、ゲノムだけでもかなり決定的になってしまっているので、誰もが容易にゲノムを読めるような時代になってきた時に、われわれはどう考えれば良いのか…。もっと難しい問題は、仮に着床前診断を日本で禁止したとしても、お金持ちは外国へ行ってやるだろうと思います。アメリカなどは基本的に功利主義ですから、「お金持ちはやっても良い」となった時に、貧富の差がその人が生涯に患うであろう病気の差にまで繋がることについての利益差を助長するのではないか…。そう考えると、なんでもかんでも法律で決めることが正しいかどうかすら、難しい時代になってくると思います。
これからは宗教家の方も、こういった問題についての相談が檀家や信徒からいっぱい持ち込まれるかもしれません。もし、1,000ドルで自分の全ゲノムが判るようになった場合、医者が一番困ると思われることは何かというと、患者との間のインフォームドコンセントに時間を取られ過ぎるのではないかという点です。実際に患者のゲノム情報を知ってあることを判断しようと思うと、患者の側にもかなりの生命科学の知識がないと難しい。最近、われわれが言っていることは、中学校ぐらいから病気とゲノムの関係などを教えておいてもらわないと、いくら医者とはいえ、患者にどこから説明すればよいのかが判りません。これは、話題提供としてお話をさせていただきました。
最後に、先程少し触れましたが、最近、本を書きました。そこそこ難しい箇所もあるので、売れないかなと心配していたのですが、おかげさまで結構売れていて初版は既に売り切れました。それならもっと増刷したらどうかと言いましたら、編集の方に「なんで売れているのか判らない場合はいつ失速するか判りませんから」と断られました(会場笑い)。けれども、今日のお話をもう少し専門的に、かつ解りやすく書いたつもりですので、もし興味がある方はお買い求めいただければと思います。
今日の話は、「生命をつくりかえることができるか」という、大胆なテーマでしたが、結論から申せば、エピジェネティックな状態を変えるリプログラミングで「ある程度は変えることができる」時代にはなってきました。しかし、これはかなり特殊な状態であります。今日の話に出てきました核移植、リプログラミング、ES細胞、山中4因子によるiPS細胞の話や、そういったことのバックグラウンドの知識としてエピジェネティクスというものがあります。エピジェネティクス、あるいはエピゲノムというのも大事ですが、やはりそれ以上に、先天的に決まってしまっているゲノムそのもののほうが大事です。仮に、10万円も出せば確実に個人のゲノム情報が手に入るような時代が到来したら、例えば自分はどのぐらい糖尿病や高血圧になりやすいのかを調べる人がいっぱい出てくるでしょう。その時、望むと望まざるとにかかわらず、宗教や医学はもとより、社会全体として皆がある程度考えなければならない時代がやってくるのではないかということを最後にお話しさせていただきました。本日の話は以上です。ご清聴有り難うございました。
(連載おわり 文責編集部)